- ja Change Region
- Global Site
創薬
ハイスループットスクリーニングやハイスループットイメージングはここ数十年、創薬試験の中心的な役割を担っており、薬剤候補選別の自動化に非常に有用な手法となっています。また、イメージングは空間的情報や経時変化を取得することができるため、ゲノミクス、プロテオミクスなどの手法を補完することができます。さらに人工知能を使用した細胞表現型プロファイリングなどの最新の技術と組み合わせることにより、光学顕微鏡を使用したイメージング・スクリーニング装置は、創薬過程においてより重要で、より身近になっていく可能性があります。ニコンは、顕微鏡をベースとしたソリューションを提供することにより、これらのニーズに対応します。
創薬に関連する製品
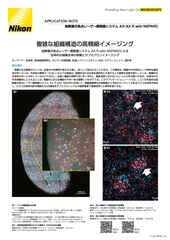
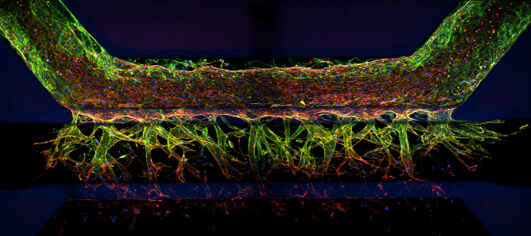
OrganoPlate® システム (MIMETAS) を使用して培養した血管新生モデルの 3D 画像
倒立顕微鏡システム
ECLIPSE Ti2-E/Ti2-LAPP:倒立顕微鏡Ti2-Eを照明モジュールTi2-LAPPや他のデバイスと同期させて操作することで、複雑な多次元画像取得が可能です。また、Ti2-EはフォーカスロックシステムであるPerfect Focus System 4 (PFS4)を装備しているため、長時間イメージングにおける高い安定性を実現します。
ECLIPSE Jiは創薬の研究開発を支援するために開発されたデジタル顕微鏡です。細胞カウントや蛍光発現効率測定、アポトーシス測定など多数の定型実験を自動で実行できるアッセイをご用意しています。面倒なピント調整や露光調整などを装置が担い、細胞単位の結果からプレート単位の結果までを分かりやすく表示しすることで実験結果の分析をサポートします。
ハイコンテントイメージング
BioPipeline LIVE/PLATE:ニコンは、ハイスループット・ハイコンテントイメージングをサポートするBioPipeline LIVEおよびBioPipeline PLATEシステムを提供しています。いずれも倒立顕微鏡ECLIPSE Ti2-Eをベースとし、ウェルプレートなどの最大44枚の容器の自動交換とイメージングに対応する搬送アームを装備。BioPipeline LIVEには、長時間のライブセルイメージングによるアッセイに対応した、インキュベーターも搭載しています。
共焦点イメージング
AX/AX R:共焦点レーザー顕微鏡システムAX/AX Rは、25 mmの広視野にわたり、最大8192 x 8192画素の高解像度画像を取得できます。AX Rは、超高速イメージング(毎秒30フレーム:2048 x 512画素、1024 x 512画素)の可能なレゾナントスキャナーを搭載し、ハイスループットスクリーニングやライブセルイメージングに対応します。
多光子イメージング
AX R MP:最新の高速多光子共焦点レーザー顕微鏡システムAX R MPは、1300 nmの励起光を用いて最大1.4 mmまでの深部をイメージングすることができ、in vivoイメージングや生体内イメージングに最適です。AX R MPは、横幅を必要とする実験系のための単支柱と奥行を必要とする実験系のための門型支柱の2タイプの専用正立顕微鏡支柱が選択できます。
ソフトウェアおよびAI技術
画像統合ソフトウェアNIS-Elements:NIS-Elementsは、顕微鏡操作、画像解析、画像処理のためのニコンの主力ソフトウェアです。NIS-Elements HCは、ハイスループット・ハイコンテントイメージングの用途に最適化されています。ヒートマップ、サンプル画像、バイナリーマスク、アッセイ結果などを一元管理できるため、迅速なフィルタリングや解析が可能です。さらに、ディープラーニングをベースとするソフトウェアモジュールNIS.aiを組み込むことで、画像セグメンテーションなどの解析に人工知能 (AI)の力を活用できます。
●:使用可能 , ⚬:オプション
| Base System | Modules | ||||
|---|---|---|---|---|---|
| 倒立顕微鏡ECLIPSE Ti2-E (落射=蛍光イメージング) |
デジタル倒立顕微鏡 ECLPSE Ji | AX R レゾナント共焦点レーザー顕微鏡システム |
Ti2-LAPP E-TIRF照明装置によるTIRFイメージング |
AX R MP 高速多光子共焦点レーザー顕微鏡システム |
|
| 相対的最大観察深度 | ~ 5 μm ~ 15 – 25 μm(デコンボリューション時) |
~ 5 μm ~ 15 – 25 μm(デコンボリューション時) |
~ 100 – 500 μm | ~ 100 – 300 nm | ~ 500 μm – 1.5 mm |
| ビデオレートでの撮影 | ●*1 | ●*1 | ●*2 | ●*1 | ●*2 |
| 視野数 | 対角25 mm(円形) | 対角25 mm(正方形) | 対角25 mm(正方形) | 対角10 mm(円形) | 対角22 mm(正方形) |
イメージング方法
| ECLIPSE Ti2-E | ECLIPSE Ji |
AX R |
Ti2-LAPP | AX R MP |
|
|---|---|---|---|---|---|
| 明視野 | Yes | Yes | No | No | No |
| ポイントスキャン共焦点 | No | No | Point-Scanning | No | Point-Scanning |
| 暗視野 | Yes | No | No | No | No |
| 微分干渉(DIC) | Yes | No | No | No | No |
| ニコンアドバンストモジュレーションコントラスト(NAMC) | Yes | No | No | No | No |
| 位相差 | Yes | No | No | No | No |
| 超解像 | No | No | NSPARC | No | No |
| 全反射照明蛍光(TIRF) | No | No | No | Yes | No |
| ボリュームコントラスト | Yes | Yes | No | No | No |
| 落射蛍光 | Yes | Yes | No | No | Yes |
使用可能な顕微鏡
| ECLIPSE Ti2-E |
ECLIPSE Ji |
AX R |
Ti2-LAPP | AX R MP |
|
|---|---|---|---|---|---|
| 倒立顕微鏡ECLIPSE Ti2-E |
No | No | Yes | Yes | Yes |
| デジタル倒立顕微鏡 ECLPSE Ji | No | No | Yes | No | No |
| 正立顕微鏡ECLIPSE Ni-E |
No | No | Yes | No | No |
| 正立顕微鏡FN1 | No | No | Yes | No | No |
| 多光子共焦点レーザー顕微鏡システム専用顕微鏡 AX-FNGP(門型支柱型) | No | No | No | No | Yes |
| 多光子共焦点レーザー顕微鏡システム専用顕微鏡 AX-FNSP(単支柱型) | No | No | No | No | Yes |
ハイコンテンツイメージングとの互換性
*1 カメラやディスク回転速度による制限あり
*2 30 fps:512 x 512スキャン
アプリケーションノート
創薬について
各創薬モデルに適した顕微鏡システム
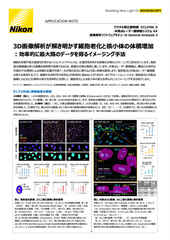
DNA(青;DAPI)、ムチン(緑;杯細胞により生成)、ソマトスタチン(赤;腸内分泌細胞により生成)で染色した小腸オルガノイドを、ポイントスキャン共焦点顕微鏡で画像取得
創薬での観察対象は、in vitroの培養接着細胞からモデル生物の全体像までさまざまです。スフェロイド、オルガノイド、オーガンチップ(臓器チップ、OoC)などの複雑な3D細胞培養モデルは、複数の細胞型で構成できるうえ、ハイスループットスクリーニングでは古典的で標準的なモデルである培養接着細胞では得ることのできない、さまざまな生理学的特性を適切に再現できます。また、オルガノイドに関しては、精密医療のために、患者由来の細胞から培養されることもあります。
落射蛍光観察は、ハイスループットスクリーニングでは標準的であるマルチウェルプレートで培養された接着細胞など、比較的平坦なサンプルに適しています。高速で感度が高く、コストもかかりません。厚みのある標本では、光学セクショニング像を撮影できる共焦点顕微鏡が有用です。
オルガノイドや組織など物理的に大きなサンプルの観察では、焦点面外のぼけ光による影響を抑えて、焦点面をより鮮明に観察するために、光学セクショニング像観察技術が必要になります。このような用途では共焦点顕微鏡の使用が一般的です。ニコンのポイントスキャン共焦点システムである共焦点レーザー顕微鏡システムAX/AX Rは、BioPipeline LIVEやBioPipeline PLATEと組み合わせることができ、サンプルの深さ数百マイクロメートルまでの光学セクショニングが取得可能です。
共焦点イメージングは、深部の光学セクショニングには適していますが、それでも不十分な場合があります。厚みのある散乱組織のin vivoイメージングでは、高速多光子共焦点レーザー顕微鏡システムAX R MPなどの多光子システムが必要となります。これにより、近赤外から赤外の光による多光子励起を利用して、焦点の合っていない蛍光や散乱光を低減することができます。
細胞解析のための、定量的位相イメージング

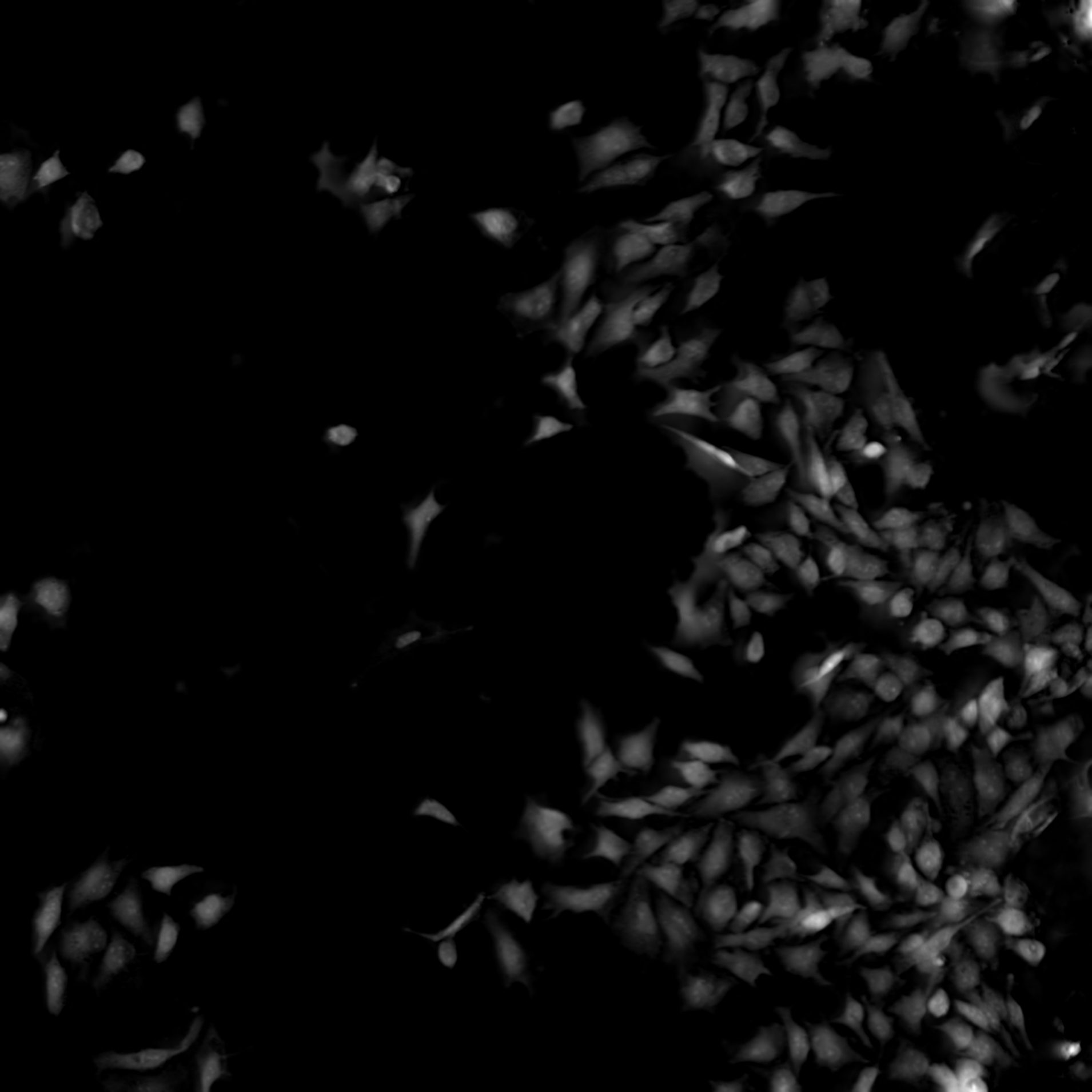
画像統合ソフトウェアNIS-Elementsの「ボリュームコントラスト」機能を使用すれば、明視野観察で3枚のZスタック画像を取得することにより、位相分布画像を生成できます。得られる位相分布画像は、光路差が最も大きい場所(培養細胞のイメージングでは細胞の中央)が最も明るくなります。この方法を使用することにより、非染色標本であっても二値化などの解析を容易に行うことができます。
「ボリュームコントラスト」機能はメニスカス効果の影響を受けません。ウェルプレートは、個々のウェルの直径が小さいため、メニスカス効果の影響が大きくなります。右の画像は、メニスカス効果がある場合の位相差画像とボリュームコントラスト処理を行った画像の比較です。
詳しくは、非染色細胞増殖アッセイにおけるボリュームコントラストの活用についてのアプリケーションノートをご参照ください。
創薬研究における人工知能の活用
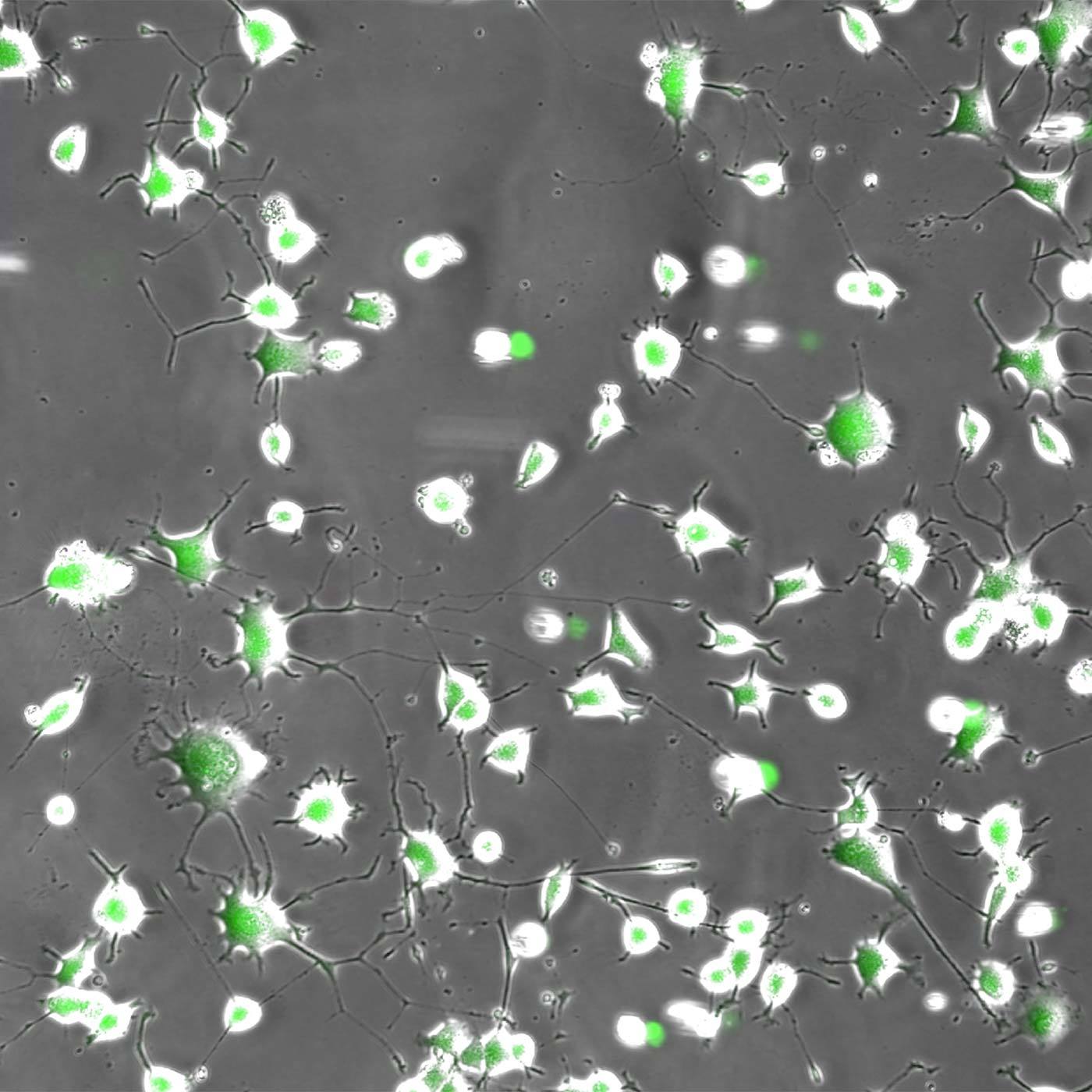

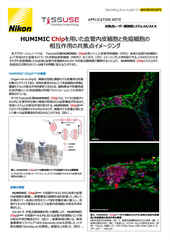
位相差画像の神経突起は、従来の二値化では正確に抽出できません。Segment.aiは手動でトレースした神経突起を学習し、対象を認識することが可能です。
画像をもとにしたアッセイの大きな利点の一つは情報量の多さです。これまでは得られた情報の一部しか活用されていませんでした。人工知能(AI)、特に人工ニューラルネットワーク(ANN)を使用したディープラーニング(DL)により、画像の特徴間のより深い相関関係を推測し、形態と表現型を特性評価することが可能になります。このような解析手法は「細胞プロファイリング」あるいは「画像に基づいたプロファイリング」と呼ばれ、非常に活発に開発が進んでいる分野です。
プロファイリングの他にも、ディープラーニングを使用して、画像解析の時間短縮や改善が可能です。ニコンは、NIS-Elementsソフトウェアで使用できるソフトウェアモジュールNIS.aiとして、ディープラーニングにもとづいた信頼性の高い画像解析ツールを設計しています。たとえば、Segment.aiは、従来の方法では分離が困難だった画像の特徴を、自動的にセグメンテーションするように学習させることができます。
創薬に活用可能なその他のNIS.aiモジュールにはConvert.aiがあります。Convert.aiは、明視野などの透過光画像のみを参照データとして、蛍光画像の特徴を予測するように学習させることができます。これは、蛍光標識による細胞毒性と、蛍光イメージングに使用する強い励起光による光毒性の、両方を低減することができます。また、Enhance.aiでは、ノイズの多い画像データから、高S/N比の画像を予測するように学習させることが可能です。このモジュールを活用することで、励起光の強度を下げ、光毒性を低減することができます。
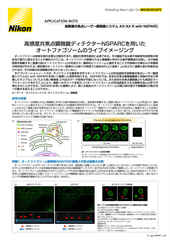
オルガノイドなどの大きなサンプルのハイスループット蛍光イメージングでは、蛍光画像から”ぼけ光”を自動的に除去するように学習済みのClarify.aiが有用です。このモジュールを活用することで、蛍光イメージングの速度のまま、共焦点システムを使用することなく光学セクショニング効果を得ることができます。
前臨床創薬研究のためのニコン受託イメージングサービス
ニコン受託研究サービスの概要
Nikon BioImaging Lab(NBIL)は、地域のバイオテクノロジー・研究コミュニティに対して受託研究サービスを提供しています。現在、米国マサチューセッツ州ケンブリッジにNBIL -Cambridge-、オランダのライデンにNBIL -Leiden-、日本の神奈川県藤沢市にNBIL -Shonan-と世界3カ所に拠点があります。これらのラボは、バイオファーマ研究分野の顧客をサポートする豊富な経験を有し、現在創薬に利用されているオルガノイドやオーガンチップ(臓器チップ、OoC)モデルを含む3D細胞培養システムの共焦点イメージングを行っています。

Nikon BioImaging Labに関する、詳細な情報やサービスの内容については、お気軽にお問い合わせください。
関連アプリケーション
用語解説
- イメージング方法
- システムのベースとして倒立顕微鏡ECLIPSE Ti2-Eを使用する場合は、Ti2-Eの項目に記載した観察方法も利用可能です。
- ビデオレートでの撮影
- ビデオレートは、通常、約30フレーム/秒(fps)と定義されていますが、 最適なイメージングレートは観察目的により異なります。一般的にEM-CCDカメラは最大60 fps(フルフレーム)で、sCMOSカメラは最大40〜100 fps(フルフレーム)で撮影可能です。
- 創薬
- 創薬とは、in vitro、ex vivo、in vivoにおける薬剤候補の確認試験や前臨床試験に着目した、複数の学問にまたがる分野です。たとえば、薬物の薬理特性を調べる一次アッセイのほか、創薬過程で検証される薬物の吸収・分布・代謝・排泄・毒性 (ADMET)および安全性に関する二次アッセイなどです。
- 相対的最大観察深度
- 十分な解像度とS/N比で画像取得できる、おおよその観察深度範囲(Z軸)を指します。この値は、サンプルや容器の光学特性や蛍光標識などにより大きく変動します。
- 視野数
- 対物レンズ倍率1倍における観察範囲の直径です。