- ja Change Region
- Global Site
アプリケーションノート
ライブセルイメージングによる細胞死経路の可視化
:ミトコンドリア膜電位とAnnexin V を活用したアポトーシスの解析
2025年11月
蛍光プローブと顕微鏡技術の発展は、医学・生物学に大きく貢献しています。生きた細胞内の分子や細胞小器官の動きをリアルタイムで観察できるようになり、細胞死経路や薬物の作用機序の解明が進みました。さらに、画像処理と解析技術の進歩により、明視野画像からラベルフリーで細胞数を計測できるようになりました。これにより、ライブセルイメージングにおける光毒性を低減しながら、細胞の形態観察や細胞数計測といった、より多くの情報を同時に取得することが可能になりました。本アプリケーションノートでは、ミトコンドリア膜電位とAnnexin Vを蛍光プローブで可視化し、Volume Contrast(VC)画像を用いてラベルフリーで細胞数を計測することで、低光毒性で初期アポトーシスを解析した例を紹介します。さらに、3つの薬剤(エトポシド、スタウロスポリン、アンチマイシンA)に対する細胞の応答性の違いについても分析しました。
キーワード:初期アポトーシス、ミトコンドリア膜電位、細胞死経路、蛍光プローブ、ライブセルイメージング、Volume Contrast、画像解析、ラベルフリーセルカウント
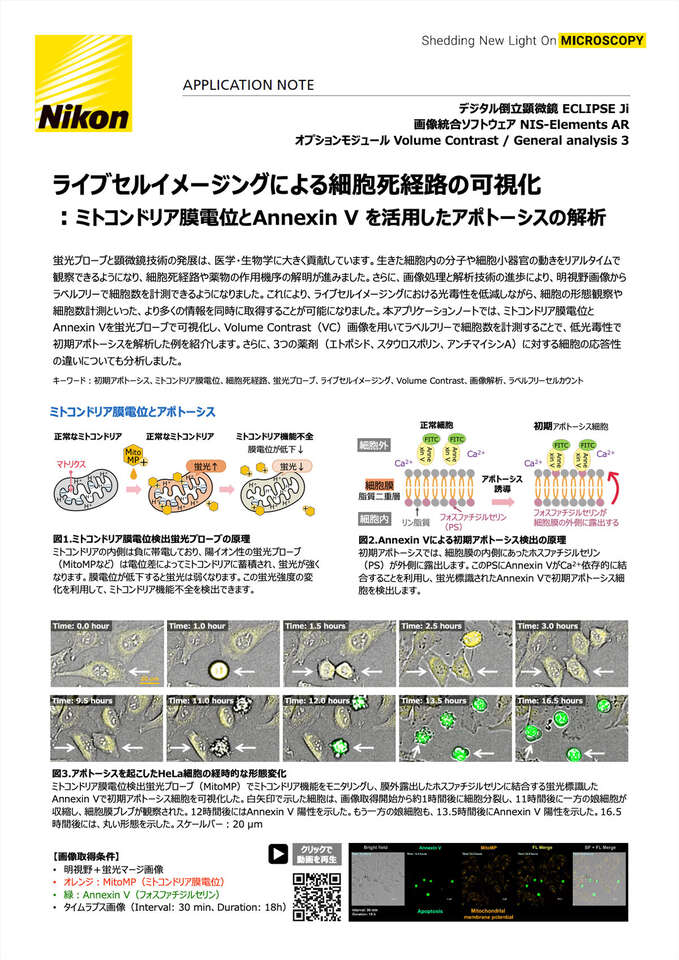
ミトコンドリア膜電位とアポトーシス
図1.ミトコンドリア膜電位検出蛍光プローブの原理
ミトコンドリアの内側は負に帯電しており、陽イオン性の蛍光プローブ(MitoMPなど)は電位差によってミトコンドリアに蓄積され、蛍光が強くなります。膜電位が低下すると蛍光は弱くなります。この蛍光強度の変化を利用して、ミトコンドリア機能不全を検出できます。
図2.Annexin Vによる初期アポトーシス検出の原理
初期アポトーシスでは、細胞膜の内側にあったホスファチジルセリン(PS)が外側に露出します。このPSにAnnexin VがCa2+依存的に結合することを利用し、蛍光標識されたAnnexin Vで初期アポトーシス細胞を検出します。
図3.アポトーシスを起こしたHeLa細胞の経時的な形態変化
ミトコンドリア膜電位検出蛍光プローブ(MitoMP)でミトコンドリア機能をモニタリングし、膜外露出したホスファチジルセリンに結合する蛍光標識したAnnexin Vで初期アポトーシス細胞を可視化した。白矢印で示した細胞は、画像取得開始から約1時間後に細胞分裂し、11時間後に一方の娘細胞が収縮し、細胞膜ブレブが観察された。12時間後にはAnnexin V 陽性を示した。もう一方の娘細胞も、13.5時間後にAnnexin V 陽性を示した。16.5時間後には、丸い形態を示した。スケールバー:20 µm
【画像取得条件】
明視野+蛍光マージ画像
オレンジ:MitoMP(ミトコンドリア膜電位)
緑:Annexin V(フォスファチジルセリン)
タイムラプス画像(Interval: 30 min、Duration: 18h)
実験の概要
HeLa細胞播種(1 x 104 cells/well, ibidi 96 well plate)、
5% CO2存在下、37℃で24時間培養
(2) 培地を除去し、MEM培地を用いて細胞を2回洗浄
(3)MEM培地で調整したMT-1 working solutionを添加し、 5% CO2存在下、37℃で30分間インキュベート
(4) 上澄みを取り除き、MEM培地を用いて細胞を2回洗浄
(5) MEM培地で調整した各種アポトーシス誘導剤を加え、細胞を処理
(6) Annexin V working solutionを添加(Annexin V – FITC stock solutionをQuenching Bufferで希釈)
染色条件の詳細については、MT-1 MitoMP Detection KitおよびAnnexin V Apoptosis Plate Assay Kitの取扱説明書をご参照下さい。
(7) ステージトップインキュベータを備えたECLIPSE Jiのステージにサンプルを設置し、30分間隔で約18時間にわたりタイムラプス画像を取得
(8) タイムラプス画像を確認後、2時間間隔で18時間のデータを抽出し、NIS-Elementsの画像解析モジュール 「General Analysis 3(GA3)」を用いて画像を数値化。
ビューアー上でグラフを表示してデータを分析。さらに、解析データをCSV形式で出力し、 Microsoft Excel® でデータを分析。
検出領域 | 蛍光ラベル | Ex/Em (nm) | 露光時間 |
|---|---|---|---|
ミトコンドリア膜電位 | MT-1 MitoMP | 550/600 | 178 ms |
フォスファチジルセリン | Annexin V -FITC | 475/515 | 215 ms |
- | None | 明視野 | 1 ms |
倍率 | 実視野(FOV) | ||
10X | 1.77 x 1.77 mm / image | ||
ポイント数 | Zスタック | ||
1ポイント/well | 6.82 µm x 3 steps (Range:13.64 µm) | ||
材料と試薬
細胞培養 | |
|---|---|
細胞 | HeLa細胞 |
増殖培地 | MEM |
培養容器 | Ibidi #89626, µ-Plate 96 Well Square |
被験物質 | |
|---|---|
化合物・ | Etoposide (0, 10, 50, 100 µM) Staurosporine (0, 0.5, 5, 10 µM) Antimycin A (0, 1, 5, 10 µM) |
試薬 | ||
|---|---|---|
製品名 | カタログ番号 | メーカー名 |
Annexin V Apoptosis Plate Assay Kit | AD12 | (株)同仁化学研究所 |
MT-1 MitoMP Detection Kit | MT13 | (株)同仁化学研究所 |
表1. 検出領域と蛍光ラベル、画像取得の条件
(C-FL-Q Quad band FL filter Cubeを使用)
Volume Contrast(VC)画像を用いたラベルフリーセルカウント
Volume Contrast(VC)は、複数のZ深度で撮影した明視野画像から蛍光画像のような位相分布画像を構築可能な、NIS-Elementsソフトウェアのアドオンモジュールです。 VC画像は、S/N (信号雑音比)が高く、背景と細胞領域の識別が容易です。これにより、セグメンテーションが簡単になり、細胞カウント用のマスクを作成して、ラベルフリーで細胞数を計測できます。Scale bar: 50 µm。
General Analysis 3(GA3)による効率的な画像解析とデータ可視化
GA3は、データの可視化に優れた多機能な画像解析モジュールです。二値化や計測に加え、グラフ表示機能も充実しています。図4では、右中央(C-1)に、ウェルプレート全体の解析結果を一覧できる「ウェルプレートビュー」を表示しています。「GA3 Main」および「GA3 Side」機能は、ミトコンドリア膜電位(オレンジ:MitoMP)とアポトーシス(緑:Annexin V)の蛍光強度変化率をウェルプレート形式で並列表示できます (図4.(C-1))。これにより、画面を切り替えることなくプレート全体の変化率を一目で確認でき、より深い考察に集中できます。 GA3の高いカスタマイズ性は、実験内容に応じた最適なデータ表示で分析を強力にサポートします。また、解析結果はExcel形式でエクスポートできるため、普段使用している統計解析ソフトウェアを用いた分析も可能です。
図4.NIS-ElementsのGA3によるミトコンドリア膜電位と初期アポトーシス解析結果表示画面の一例
(A) セルカウントマスクをオーバーレイした画像 (スケールバー:100µm)
(B) 薬剤の用量反応曲線
(C-1, C-2, C-3) ウェルプレート形式のグラフ表示 (Stacked Layout) 。黄色点線枠のアイコンを選択し、複数のグラフを切り替えて表示可能
(C-1) 各ウェルにおける蛍光強度変化率の折れ線グラフ(左:MitoMP、右:Annexin V)
(C-2) 左:各ウェルの薬剤情報 (薬剤名、濃度)、右:T=14h時点における蛍光強度変化率の棒グラフ (MitoMP (オレンジ) と Annexin V (青))
(C-3) 左:各ウェルにおける細胞数変化率の折れ線グラフ、右:T=14h時点における細胞数変化率のヒートマップ
(D) 左:全ウェルのデータテーブル、右:選択中の画像におけるMitoMPおよびAnnexin Vの蛍光強度変化率の折れ線グラフ
(E-I) 画像(A)の白色点線枠内の拡大画像
(E) 明視野画像
(F-H) 蛍光画像(F:MitoMP、G:Annexin V 、H:蛍光マージ画像)
(I) 明視野と蛍光のマージ画像にセルカウントマスク(ピンク)をオーバーレイした画像、(E-Iのスケールバー:20 µm)
タイムラプス解析の重要性
Antimycin Aは、MitoMPの蛍光強度が約2時間で急激に低下したことから、ミトコンドリア機能不全を引き起こしていることが分かります。薬剤に対する細胞の反応は予測が困難なため、ライブセルイメージングの自動撮影は非常に有効です。これにより、長時間の連続観察が可能となり、薬剤が細胞に与える変化や、その反応のタイミング、影響を正確に捉えることができます。
結果と考察
図5.タイムラプス画像と解析結果
3種類の薬剤に対する反応性を比較した画像:
(A,B,I) Etoposide 100 µM
(C,D,J) Staurosporine 10 µM
(E,F,K) Antimycin A 10 µM
(G,H,L) コントロール(薬剤未処理)
(A,C,E,G) 明視野画像
(B,D,F,H,I-L) 蛍光マージ画像(オレンジ:MitoMP、緑:Annexin V)
(A-H) 上段:T=0h、下段:T=18h
(I-L) T=18hの画像
スケールバー: (A-H) 20 µm 、 (I-L) 100 µm
グラフ:時系列折れ線グラフ
上段:細胞数変化率
中段:MitoMPの平均蛍光強度変化率
下段:Annexin Vの平均蛍光強度変化率
(M) Etoposide
(N) Staurosporine
(O) Antimycin A
HeLa細胞に対する3種の薬剤はそれぞれ特徴的な応答パターンを示しました。Etoposideは高濃度でアポトーシスを引き起こすものの作用は比較的穏やかで、Staurosporineは少量でも速やかにアポトーシスを誘導する強力な薬剤でした(図5.(M,N,下段))。Antimycin Aは、ミトコンドリア機能不全が最も顕著でした(図5(O,中段)) 。Etoposide (100 µM) は処理から12時間以降にAnnexin Vの蛍光強度が徐々に増加し、アポトーシスを誘導しました(図5.(M))。Staurosporine (10 µM) は即座に細胞が収縮し、撮影開始(T=0)時点で既に形態変化が確認されました(図5.(C, 上段))。 Antimycin A (10 µM) は、即座にMitoMPの蛍光強度が低下し、撮像開始時点で既にミトコンドリア膜電位の低下が確認されました(図5.(F, 上段))。 また、Antimycin A (10 µM) は処理から2時間以内にミトコンドリア膜電位(ΔΨm)の喪失が確認されました(図5.(O, 中段))。 通常、ミトコンドリアの機能不全は、細胞死や増殖抑制を引き起こしますが、今回の短期観察(18時間)では細胞数が約1.3倍に増加しました。これは、ワールブルグ効果による代謝シフトが関与していると考えられます。
- ミトコンドリア膜電位の低下: Antimycin Aは、ミトコンドリアの電子伝達系複合体IIIを阻害する薬剤です。プロトン勾配の形成を妨げることでミトコンドリア膜電位(ΔΨm)を急速に低下させます。これにより、酸化的リン酸化によるATP産生は停止したと推察されます。
- 解糖系へのエネルギー代謝シフト: がん細胞であるHeLa細胞は、酸化的リン酸化に依存せず、主に解糖系によってエネルギー(ATP)を生産しています。この現象は「ワールブルグ効果」として知られています。
したがって、今回の実験では、Antimycin A処理によってトコンドリアの膜電位が低下しましたが、HeLa細胞は解糖系を亢進させることで、18時間という短期間の細胞増殖に必要なエネルギーを供給し続けることができたと考えられます。しかし、長時間のAntimycin A処理は、最終的に細胞死(アポトーシスやネクローシス)を引き起こし、細胞数を減少させることが多くの研究で報告されています。
表2:各薬剤の高濃度における18時間後の変化率(初期値比)と薬剤応答性の比較
今回の実験は初期アポトーシスに焦点を当てており、18時間のタイムラプスイメージングでデータを取得しました。この18時間におよぶイメージングにおいても、使用した蛍光プローブ MitoMP(MT-1)は、コントロールウェルでの蛍光強度の低下がわずか10%に留まり、光退色が非常に少なく高精度な結果が得られました。後期アポトーシスやネクローシスといった、より後期の細胞死を指標に解析を行う場合は、死細胞検出蛍光プローブ(PI:ヨウ化プロピジウム)を共染色し、観察時間を延長することで解析が可能です。さらに、ROS(活性酸素種)検出プローブなどを組み合わせることで、細胞死経路のより詳細なメカニズム解明につながります。蛍光プローブと顕微鏡技術の発展は、医学、薬学、生物学のさらなる発展に大きく貢献しています。
その他、細胞死研究用の関連蛍光プローブ
製品名 | カタログ番号 | メーカー名 |
|---|---|---|
-Cellstain®- PI solution | P378 | (株)同仁化学研究所 |
ROS Assay Kit -Highly Sensitive DCFH-DA- | R252 | (株)同仁化学研究所 |
謝辞
実験協力・サンプル提供:株式会社 同仁化学研究所
アポトーシス誘導に関する実験条件およびイメージングに最適化された染色プロトコルの確立にご協力いただきました、株式会社同仁化学研究所の小松恭佳様をはじめ、関係者の皆様に心より感謝申し上げます。
著者情報
株式会社 ニコン 小林千春
Product Information
ECLIPSE Jiは、NIS-Elements ARと組み合わせることで、自由度の高い実験を可能にします。要望に応じて柔軟にカスタマイズできるため、個々の研究ニーズに合わせて実験を最適化できます。また、ステージトップインキュベータを設置すれば、タイムラプス画像取得によるライブセルイメージングにも対応します。
NIS-Elements ARは、JOBS/GA3モジュールと組み合わせることで、ハイコンテントイメージングを強力にサポートします。画像の取得から解析まで、シームレスなワークフローで実験を自動化し、研究を加速します。
画像解析ソフトウェアモジュール General Analysis 3(GA3)
GA3は、画像解析の自動化と効率化を実現するツールです。ノード(解析ブロック)単位で解析フローを視覚的に構築でき、画像処理からデータ解析までを自動化。画像処理、セグメンテーション、計測、グラフ表示、NIS.aiなど多様な機能を柔軟に組み合わせ可能。実験に最適な形でデータを表示し、解析を強力にサポートします。
