- ja Change Region
- Global Site
アプリケーションノート
超解像顕微鏡N-STORMが捉えたSARS-CoV-2 感染細胞内のウイルス粒子構成タンパク質
2023年11月
SARS-CoV-2の増殖メカニズムの解明は、COVID-19の予防や治療法の開発に重要である。SARS-CoV-2感染細胞の内部では、新しいウイルス粒子が形成されるまでの間に、各ウイルス構成タンパク質の発現量とその比率、細胞内局在が時間経過とともに変化する。特に内腔小胞を有するエンドソーム(Multivesicular body; MVB)やリソソームは、ウイルス粒子形成の場として注目される一方で、それらに各ウイルス構成タンパク質が集積する過程については不明な点が多い。
順天堂大学大学院医学研究科脳回路形態学の石田葉子先生、岡本慎一郎先生、髙橋慧先生、日置寛之先生らは、直径60–100 nmのSARS-CoV-2を構成するタンパク質のうち、スパイクタンパク質(Sタンパク質)とヌクレオカプシドタンパク質(Nタンパク質)に着目し、MVBやリソソーム内における Sタンパク質とNタンパク質の局在を、共焦点顕微鏡および超解像顕微鏡N-STORMを用いて観察している。
本アプリケーションノートでは、日置先生らがN-STORMを用いて捉えることに成功した、SARS-CoV-2感染細胞内のウイルス粒子構成タンパク質の超解像画像を紹介する。
キーワード: SARS-CoV-2、COVID-19、スパイクタンパク質(Sタンパク質)、ヌクレオカプシドタンパク質(Nタンパク質)、超解像顕微鏡N-STORM
概要
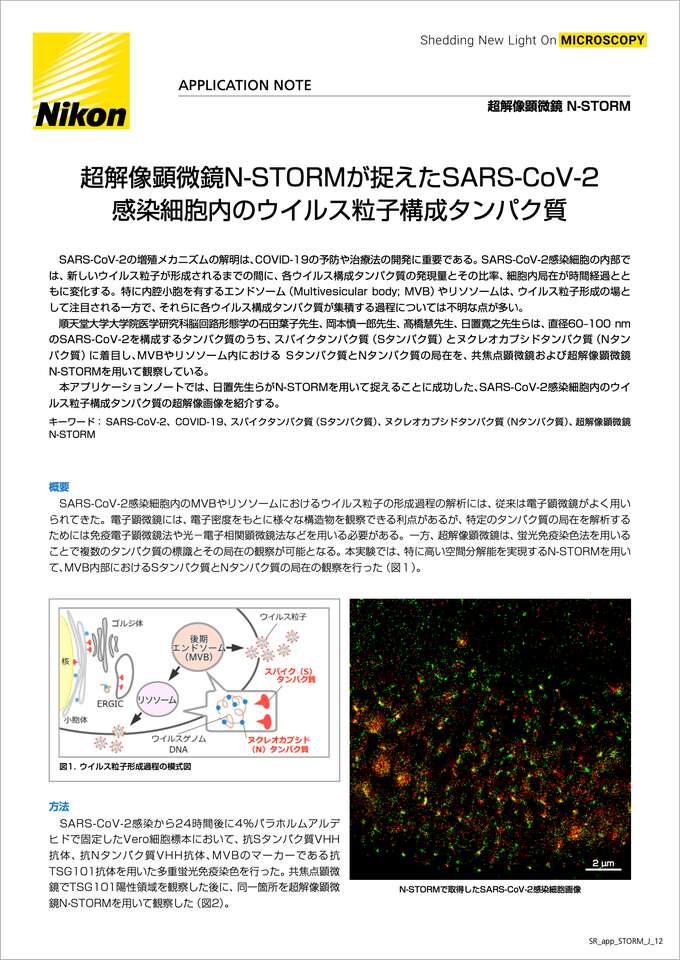
SARS-CoV-2感染細胞内のMVBやリソソームにおけるウイルス粒子の形成過程の解析には、従来は電子顕微鏡がよく用いられてきた。電子顕微鏡には、電子密度をもとに様々な構造物を観察できる利点があるが、特定のタンパク質の局在を解析するためには免疫電子顕微鏡法や光-電子相関顕微鏡法などを用いる必要がある。一方、超解像顕微鏡は、蛍光免疫染色法を用いることで複数のタンパク質の標識とその局在の観察が可能となる。本実験では、特に高い空間分解能を実現するN-STORMを用いて、MVB内部におけるSタンパク質とNタンパク質の局在の観察を行った(図1)。
図1.ウイルス粒子形成過程の模式図
N-STORMで取得したSARS-CoV-2感染細胞画像
方法
SARS-CoV-2感染から24時間後に4%パラホルムアルデヒドで固定したVero細胞標本において、抗Sタンパク質VHH抗体、抗Nタンパク質VHH抗体、MVBのマーカーである抗TSG101抗体を用いた多重蛍光免疫染色を行った。共焦点顕微鏡でTSG101陽性領域を観察した後に、同一箇所を超解像顕微鏡N-STORMを用いて観察した(図2)。
共焦点顕微鏡
超解像顕微鏡 N-STORM
図2.共焦点顕微鏡と超解像顕微鏡N-STORMで捉えたSARS-CoV-2感染細胞画像
(A):共焦点顕微鏡で取得した画像。
共焦点システム:A1R HD25、対物レンズ:CFI Apochromat Lambda S 60X Oil(NA 1.4)
(B):(A)と同一視野を超解像顕微鏡N-STORMで取得した画像。
(C):(B)の一部を拡大した画像。対物レンズ : CFI SR HP Apochromat TIRF 100XC Oil(NA 1.49)
緑:Sタンパク質(ATTO647)、赤:Nタンパク質 (Alexa Fluor 568)
結果
共焦点顕微鏡で感染細胞を観察したところ、Sタンパク質およびNタンパク質に対応する蛍光シグナルのほとんどが共存していた(図2A)。次に、同一視野を超解像顕微鏡N-STORMを用いて観察したところ、Sタンパク質およびNタンパク質の細胞内局在をより高解像度で捉えることができた(図2B)。さらにその拡大像では、Sタンパク質およびNタンパク質に由来する蛍光シグナルは点状となっており、一つ一つの輝点を分離して観察できた(図2C)。
まとめ
超解像顕微鏡は光の回折限界を越えた微細構造の観察を可能とする手法であり、従来は電子顕微鏡でしか観察できなかった超微形態の光学的な観察を実現した。さらにN-STORMを用いることで、多種類の抗原の局在分布を高い解像度で比較的容易に観察可能となった。今回、SARS-CoV-2感染細胞の超微形態の観察を行った結果、Sタンパク質とNタンパク質の細胞内分布を高い解像度で捉えることができた。これらの技術を用いることで、ウイルス粒子構成タンパク質の細胞内局在を高い精度で解析することが可能となり、ウイルス粒子形成メカニズムの解明に貢献することが期待される。
謝辞
順天堂大学大学院医学研究科脳回路形態学の石田葉子先生、岡本慎一郎先生、髙橋慧先生、日置寛之先生には、アプリケーションノート作成にあたり、画像のご提供ならびに研究内容に関してご教示いただきましたこと、深謝致します。また、筑波大学医学医療系感染生物学部門分子ウイルス学分野の川口淳史教授には、SARS-CoV-2感染Vero細胞標本をご提供いただきましたこと、深謝致します。
なお、ウイルス感染症に関する基礎研究への一助として光学顕微鏡を用いた高度な画像解析などを行う取り組みに対し、株式会社ニコンが寄付を実施した研究における成果の一部です。
参考文献
Correlative multi-scale cryo-imaging unveils SARS-CoV-2 assembly and egress.
Mendonça et al.
Nat. Commun., 2021;12(1):4629.
https://www.nature.com/articles/s41467-021-24887-y
SARS-CoV-2 nucleocapsid protein adheres to replication organelles before viral assembly at the Golgi/ERGIC and lysosome-mediated egress.
Scherer et al.
Sci. Adv., 2022;8(1):eabl4895.
https://www.science.org/doi/10.1126/sciadv.abl4895
製品情報
超解像顕微鏡 N-STORM
ローカリゼーション法の一つであるSTORM(Stochastic Optical Reconstruction Microscopy)を採用し、従来の光学顕微鏡の約10倍の解像度を実現した。細胞内小器官の構造を1分子レベルで観察することが可能。
水平解像度:約20 nm
Z軸方向解像度:約50 nm
