- it Change Region
- Global Site
- Casa
- Applicazioni
- Scienze della vita
- Scoperta di nuovi farmaci
Scoperta di nuovi farmaci
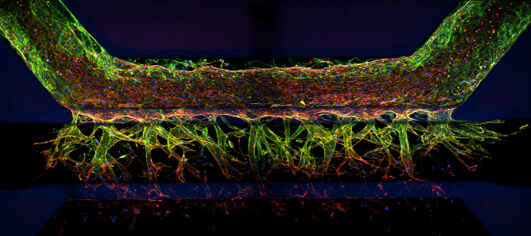
L’high-throughput screening/imaging ha occupato una posizione centrale nei test per la scoperta di farmaci negli ultimi due decenni, fornendo opzioni automatizzate e altamente quantitative per lo screening di un gran numero di composti candidati come hits. Inoltre, l'imaging integra la genomica, la proteomica e altri metodi di “-omica” fornendo un contesto spaziale. In combinazione con tecniche avanzate come il profiling del fenotipo cellulare tramite intelligenza artificiale, l'imaging/screening basato su microscopi ottici sembra destinato a diventare una componente ancora più importante (e accessibile) del processo di scoperta dei farmaci. Nikon di conseguenza si impegna a fornire soluzioni di basate su prodotti di microscopia per soddisfare queste esigenze.
Prodotti per il Scoperta di nuovi farmaci
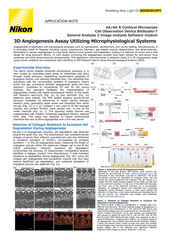
Stack di immagini 3D di un modello di angiogenesi coltivato utilizzando il sistema OrganoPlate® (MIMETAS).
Sistemi di microscopi invertiti
ECLIPSE Ti2-E / Ti2-LAPP: il funzionamento sincronizzato del microscopio invertito Ti2-E con i moduli di illuminazione Ti2-LAPP e altri dispositivi hardware consente acquisizioni di immagini multidimensionali complesse. Inoltre, il Ti2-E è dotato del sistema di blocco della messa a fuoco Perfect Focus System 4 (PFS4), che fornisce il massimo livello di stabilità per l'imaging esteso.
Imaging confocale
AX / AX R: i sistemi confocali a scansione puntiforme AX / AX R sono in grado di acquisire immagini su un ampio campo visivo di 25 mm con una risoluzione fino a 8192 x 8192 pixel. L'AX R è dotato di uno scanner risonante in grado di acquisire immagini ad altissima velocità (2048 x 512 pixel, 1024 x 512 pixel: 30 fotogrammi al secondo), che supporta lo screening high throughput, l'imaging live e altro ancora.
Sistemi confocali a disco rotante serie CSU: i confocali a disco rotante CSU-W1 e CSU-W1 SoRa di Yokogawa possono essere tutti configurati sui sistemi BioPipeline PLATE e LIVE, fornendo opzioni confocali flessibili e adatte alle cellule vive per imaging ad alto contenuto.
Imaging multifotonico
AX R MP: AX R MP è l'ultimo sistema multifotone di Nikon, che fornisce immagini profonde fino a 1,4 mm nel campione utilizzando una luce di eccitazione di 1300 nm, che lo rende ideale per l'imaging in vivo e intravitale tardivo. Sono disponibili due supporti per microscopi verticali per l'uso con AX R MP: il supporto singolo per campioni ampi e il supporto “a cancello” per campioni profondi.
Software e intelligenza artificiale
Software NIS-Elements: NIS-Elements è il software integrato principale di Nikon per il funzionamento del microscopio, l'analisi delle immagini e la loro visualizzazione. NIS-Elements HC è ottimizzato per applicazioni di imaging high throughput e ad alto contenuto. Heatmaps, immagini di campioni, maschere binarie, risultati di test e altro ancora possono essere gestiti centralmente per velocizzare il filtraggio e l’analisi. Inoltre, i moduli software basati sul deep learning NIS.ai possono essere incorporati per sfruttare la potenza dell'intelligenza artificiale (AI) in analisi come la segmentazione delle immagini.
●: included, ⚬: option
| Base System | Modules | ||||||
|---|---|---|---|---|---|---|---|
| ECLIPSE Ti2-E Inverted Microscope (Widefield Imaging) |
ECLIPSE Ji Digital Inverted |
AX R Resonant Confocal System |
Ti2-LAPP E-TIRF Illuminator |
AX R MP Multiphoton Microscope System |
CSU-W1 Spinning Disk Confocal Scanner |
CSU-W1 SoRa Spinning Disk Super-Resolution System |
|
| Limite relativo di profondità dell’imaging | ~ 5 μm ~ 15 – 25 μm (with deconvolution) |
~ 5 μm ~ 15 – 25 μm (with deconvolution) |
~ 100 – 500 μm | ~ 100 – 300 nm | ~ 500 μm – 1.5 mm | ~ 50 – 100 μm | ~ 50 – 100 μm |
| Supporta l'imaging video-rate | ●*1 | ●*1 | ●*2 | ●*1 | ●*2 | ●*3 | ●*3 |
| Campo visivo | 25 mm diagonal (circular) | 25 mm diagonal (square) | 25 mm diagonal (square) | ~ 10 mm diagonal (circular) | 22 mm diagonal (square) | 17 x 16 mm (rectangular) | 17 x 16 mm (rectangular) |
Modalità di imaging supportate
| ECLIPSE Ti2-E |
ECLIPSE Ji |
AX R | Ti2-LAPP | AX R MP | CSU-W1 | CSU-W1 SoRa |
|
|---|---|---|---|---|---|---|---|
| Brightfield | Yes | Yes | No | No | No | No | No |
| Confocal | No | No | Scansione puntiforme | No | Scansione puntiforme | Spinning Disk | Spinning Disk |
| Darkfield | Yes | No | No | No | No | No | No |
| DIC | Yes | No | No | No | No | No | No |
| Nikon Advanced Modulation Contrast (NAMC) | Yes | No | No | No | No | No | No |
| Phase Contrast | Yes | No | No | No | No | No | No |
| Super-Resolution | No | No | Microscopia a scansione di immagini | No | No | No | Riassegnazione dei pixel ottici |
| TIRF | No | No | No | Yes | No | No | No |
| Volume Contrast | Yes | Yes | No | No | No | No | No |
| Widefield Fluorescence | Yes | Yes | No | No | Yes | No | No |
Compatible Microscope Stands
Ti2-E |
ECLIPSE Ji |
AX R | Ti2-LAPP | AX R MP | CSU-W1 | CSU-W1 SoRa |
|
|---|---|---|---|---|---|---|---|
| ECLIPSE Serie ECLIPSE Ti2 invertita |
No | No | Ti2-E | Ti2-E | Ti2-E | Yes | Yes |
| ECLIPSE Ji Digital inverted |
No | No | Yes | No | No | No | No |
| ECLIPSE Ni Series Upright | No | No | Ni-E | No | No | Yes | No |
| ECLIPSE FN1 Upright |
No | No | Yes | No | No | Yes | No |
| AX-FNGP Upright | No | No | No | No | Yes | No | No |
| AX-FNSP Upright | No | No | No | No | Yes | No | No |
*1 Limitato dal sistema di telecamere
*2 30 FPS con scansione 512 x 512
*3 Limitato dal sistema della telecamera e dalla velocità di rotazione del disco
Letteratura correlata
Discussion of Scoperta di nuovi farmaci
Selecting a Microscope System for your Drug Discovery Model
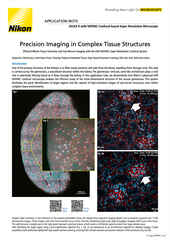
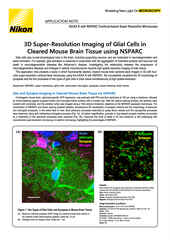
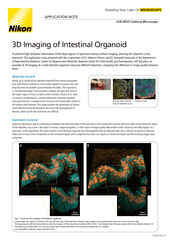
Intestinal organoid stained for DNA (blue; DAPI), mucin (green; produced by goblet cells), and somatostatin (red; produced by enteroendocrine cells), imaged using point-scanning confocal microscopy.
Model systems for drug discovery run just about the entire range of possibility, from in vitro adherent cell cultures to whole model organisms and almost everything in between. Complex 3D cell culture models such as spheroids, organoids, and organs-on-chips can be composed of multiple cell types to better recapitulate various physiological characteristics lost in traditional adherent cell cultures, which are the traditional standard for high throughput screening. Additionally, organoids can even be cultured from autologous (patient-derived) cells for developing precision medicines.
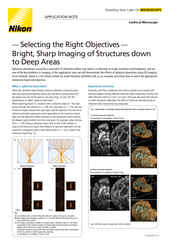
Widefield fluorescence imaging is an appropriate choice for relatively flat samples, such as adherent cells cultured in multi-well plates, the traditional standard for high throughput screening. It is fast, sensitive, and cost effective, but does not provide intrinsic optical sectioning – the ability to effectively image a single plane in a thick 3D specimen.
Physically larger 3D models, such as organoids and tissue, may require an imaging technique with optical sectioning capabilities to capture the features of interest without being overly compromised by out-of-focus blur. Confocal microscopy is the standard for such applications, Nikon offers the AX / AX R confocal microscopes, point-scanning systems for imaging discrete sections up to several hundred micrometers deep in various samples.
While confocal imaging is a suitable choice for optical sectioning at depth, sometimes it is insufficient. In vivo imaging in the presence of thick and scattering tissues often necessitates the use of multiphoton imaging, such as the Nikon AX R MP multiphoton microscope system, which uses multiphoton excitation with near-infrared to infrared light to minimize out-of-focus excitation and scattering.
Quantitative Phase Imaging for Cell Analysis

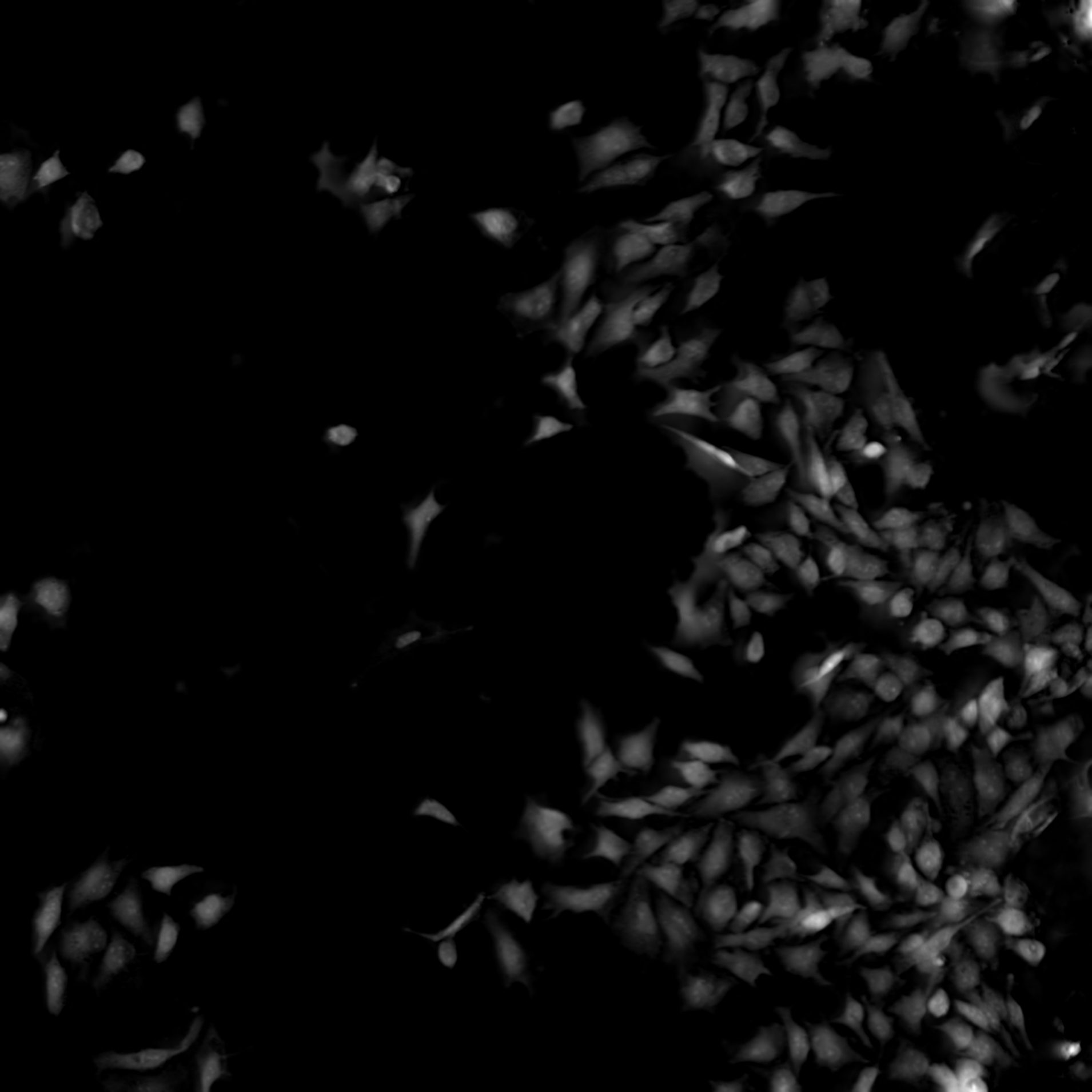
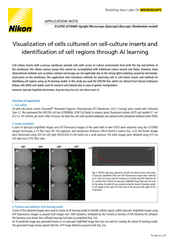
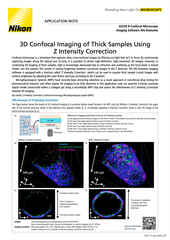
Nikon’s ECLIPSE Ti2-E inverted microscope, which forms the base of the BioPipeline LIVE and BioPipeline PLATE systems, is capable of quantitative phase imaging via the Nikon Volume Contrast technique, which only requires a small Z stack of brightfield images (as few as three images per stack) to create the phase distribution image. The resulting phase distribution image is brightest where the optical path difference is greatest – in the middle of the cell when imaging a culture. This is beneficial for cell segmentation via thresholding and other methods.
Unlike other transmitted light (diascopic) imaging techniques, such as phase contrast, Volume Contrast is unaffected by the meniscus effect, which can be significant in well plates due to the small diameter of individual wells. Performance of phase contrast and Volume Contrast in the presence of a meniscus is compared in the image on the right.
For more information, see our recent application note detailing the use of Volume Contrast as part of a label-free cell proliferation assay, a commonly performed assay in drug discovery research.
Enhancing Drug Discovery Research using Artificial Intelligence
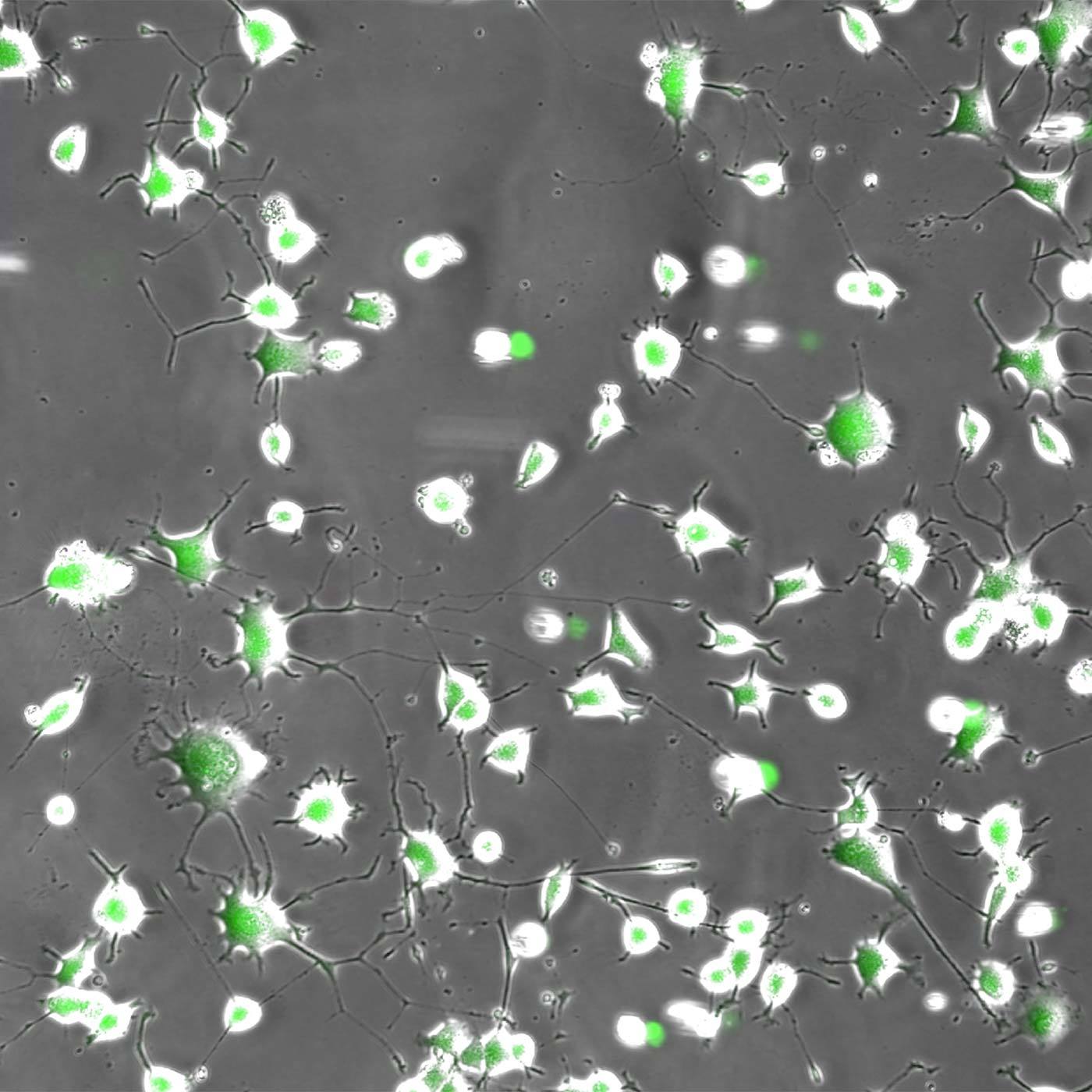

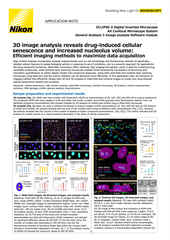
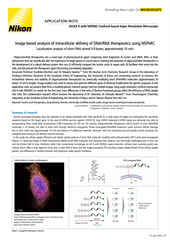
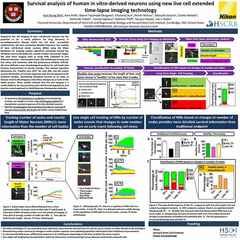
Neurites in phase-contrast were not possible to define accurately by traditional thresholding. Segment.ai was trained on hand-traced neurites (human recognized) and learned how to trace neurites in subsequent images.
One of the great advantages of image-based assays is their rich information content. Until recently, however, relatively little of this information could be leveraged in a practical manner. However, new approaches based on artificial intelligence (AI), and particularly deep learning (DL) methods using artificial neural networks (ANNs), allow for deeper correlations between image features to be inferred and applied towards characterizing morphology and phenotype. Such analytical approaches have been referred to as “cell profiling” or “image-based profiling,” and represent a very active area of development.
In addition to profiling, DL can be used to help accelerate and strengthen image analyses in other ways. Nikon is committed to the design of reliable DL-based image analysis tools under the umbrella of NIS.ai – a series of software modules available for the NIS-Elements software. For example, the Segment.ai module can be trained to automatically segment difficult image features that are difficult to isolate using classical approaches.
Other NIS.ai modules of potential application for drug discovery work includes Convert.ai, which can be trained to predict image features from a fluorescence channel using only a brightfield or another transmitted light channel as a reference, which can help cut down on both cytotoxicity (from the fluorescent label) and phototoxicity (from the high intensity light used for fluorescence imaging). Relatedly, the Enhance.ai module can be trained to predict a higher signal-to-noise version of noisy image data. This allows for a reduction in illumination intensity, and thus phototoxicity.
High throughput widefield fluorescence imaging of larger model systems, such as organoids, can benefit from our Clarify.ai module, which is pre-trained to provide automatic blur removal from widefield fluorescence microscopy images. This allows for users to benefit from the speed of widefield fluorescence imaging, but with enhanced optical sectioning and without the need for a confocal system.
Nikon Contract Imaging Services for Pre-Clinical Drug Discovery Research
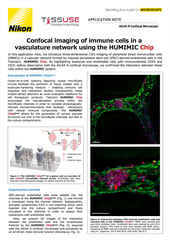
Nikon contract research services at a glance.
The Nikon BioImaging Labs provide contract research services to their local biotech and research communities, as well as remote services* for clients located elsewhere. With locations in Cambridge, MA, USA, Leiden, The Netherlands, and Shonan, Japan, the Nikon BioImaging Labs have significant experience working with customers in the biopharma research space and performing confocal microscopy of organoids and other 3D cell culture systems now used for drug discovery studies, including various commercially produced organ-on-chip models.

The Nikon BioImaging Labs are not only capable of data acquisition, but their full-service capabilities also extend to assay design, assay development, assay validation, cell culture, sample preparation, and data analysis. If you would like to learn more and see if services at one of the Nikon BioImaging Labs is right for you, please don’t hesitate to contact us to set up a free consultation.
* The service may vary depending on the facility. Please contact the Nikon BioImaging Lab near your location for details.
Related Solutions
Glossario
- Campo visivo
- Il campo visivo del sistema, indicato anche come numero di campo, è il diametro dell'area di imaging con un ingrandimento nominale di 1X.
- Limite relativo di profondità dell’imaging
- Indica l'intervallo approssimativo di profondità Z (assiale) all'interno del quale il sistema indicato può fornire immagini con qualità di sezionamento ottico e rapporto segnale-rumore sufficienti. Questo valore può essere piuttosto variabile e dipende notevolmente dalle proprietà ottiche del campione e del recipiente, nonché dal labeling.
- Modalità di imaging supportate
- Le varie tecniche di imaging al microscopio offerte da ciascun sistema. Si ricorda che quasi tutte le modalità di imaging supportate dal microscopio invertito ECLIPSE Ti2-E rimangono accessibili quando viene utilizzato come base per uno qualsiasi degli altri sistemi elencati in questa tabella.
- Scoperta di nuovi farmaci
- La scoperta di farmaci è un campo interdisciplinare incentrato sull'identificazione e la sperimentazione preclinica di potenziali farmaci in vitro, ex vivo ed in vivo. Ciò include analisi primarie delle proprietà farmacologiche del farmaco, nonché analisi secondarie di assorbimento, distribuzione, metabolismo, eliminazione e tossicologia (ADMET) e relativi fattori di sicurezza che vengono valutati nel processo di scoperta.
- Supporta l'imaging video-rate
- La modalità “video rate” (frequenza video) è tradizionalmente definita come circa 30 fotogrammi al secondo (FPS). La velocità di imaging ottimale dipende dall'applicazione e può essere più veloce o più lenta di 30 FPS. Le telecamere EM-CCD in genere possono acquisire immagini fino a 60 FPS (full frame) e le telecamere sCMOS fino a 40-100 FPS (full frame).
- Casa
- Applicazioni
- Scienze della vita
- Scoperta di nuovi farmaci