- pt Change Region
- Global Site
- Início
- Aplicações
- Ciências da vida
- Aquisição de Imagem em Nanoescala
Aquisição de Imagem em Nanoescala
Por centenas de anos, a resolução da microscopia de luz foi fundamentalmente limitada pela difração, com ~200 nanômetros (nm) sendo considerado o limite aproximado em XY. Esse limite pode ser suficiente para observar células individuais e algumas características subcelulares, mas é insuficiente para visualizar minuciosamente detalhes de estruturas menores de organelas e biomoléculas únicas, que geralmente têm dimensões em um único nm.
A história recente testemunhou a invenção de vários métodos de aquisição de imagem óptica de “super-resolução”, que exploram diferentes estratégias para contornar o limite imposto pela difração. A importância da super-resolução foi reconhecida com o Prêmio Nobel de Química de 2014 e já contribuiu para diversas descobertas, como a estrutura do citoesqueleto periódico do axônio.
Produtos para Aquisição de Imagem em Nanoescala
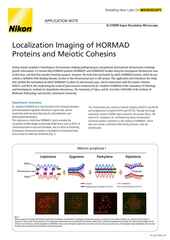
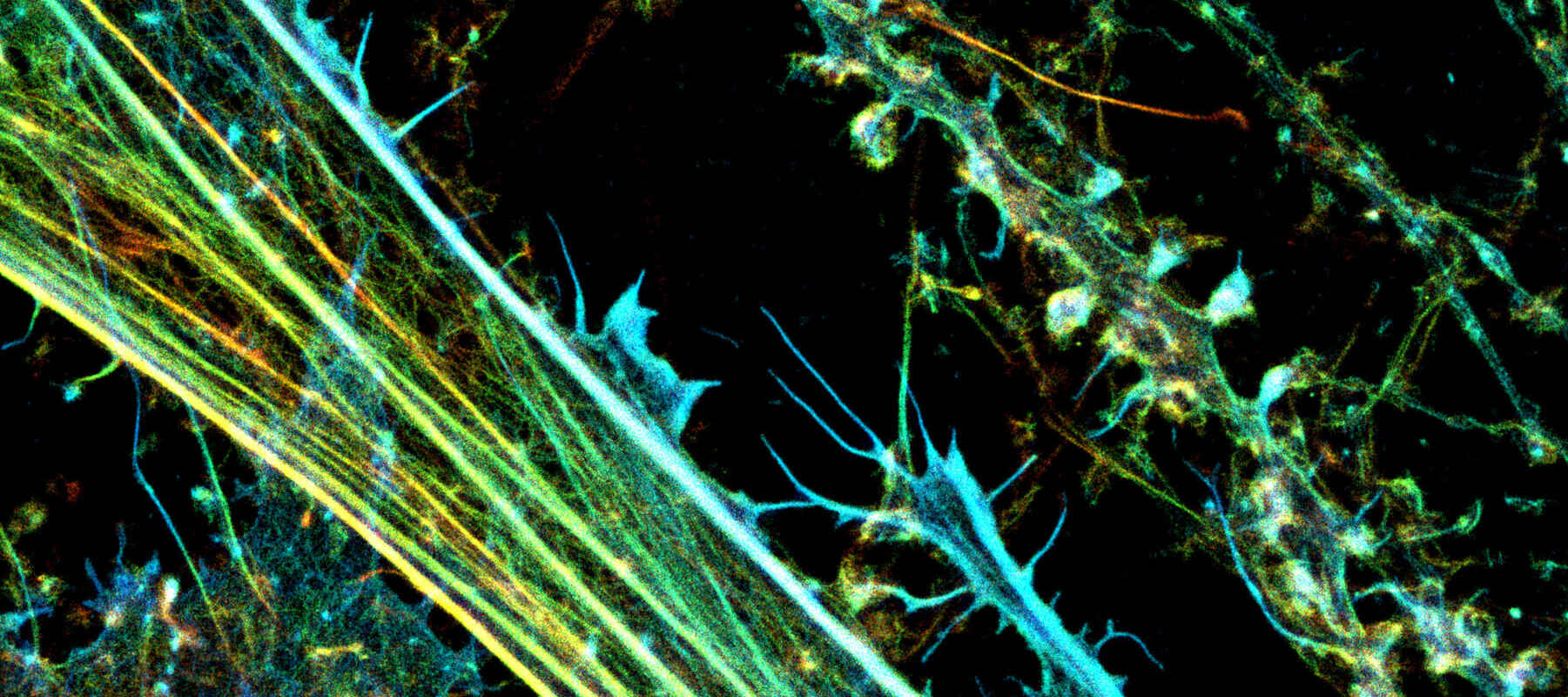
Imagem 3D-STORM de uma cultura neuronal com marcação fluorescente (codificada por cores para profundidade), adquirida pelo Prof. Christophe Leterrier (CR1 CNRS) utilizando um sistema Nikon N-STORM.
O sistema de microscópio de super-resolução N-STORM da Nikon fornece a mais alta resolução entre todos os sistemas oferecidos pela empresa, de aproximadamente uma ordem de magnitude maior em comparação com a epifluorescência de campo amplo em XYZ. O N-STORM é configurado no microscópio invertido Ti2-E, que fornece alta estabilidade graças ao sistema de travamento de foco Perfect Focus System 4 (PFS4), que também é utilizado para deslocamento axial preciso em nosso modo STORM de aquisição de imagem em série Z, permitindo a aquisição de imagens de estruturas de até ~5 µm de espessura. A aquisição de imagem convencional de fluorescência de reflexão interna total (TIRF) também é possível por meio do N-STORM.
O sistema confocal de disco giratório de super-resolução Yokogawa CSU-W1 SoRa é um instrumento confocal de disco giratório que integra um disco de microlente de emissão para obter super-resolução por reatribuição de pixel óptico. Como o CSU-W1 SoRa apresenta um design de disco giratório, a aquisição de imagem é rápida.
●: Incluído, ⚬: Opcional
N-STORM | Yokogawa CSU-W1 SoRa | |
|---|---|---|
Limite relativo de resolução óptica | ~20 nm (XY)* | ~120 nm (XY)* |
Limite relativo de profundidade da aquisição de imagem | ~ 5 μm | ~ 50 – 100 μm |
Taxa de aquisição de imagem suportada | ~0.1 FPS | ~30+ FPS |
Canais espectrais suportados | 3 | 6 |
Área máxima de aquisição de imagem | 80 x 80 μm | 61 x 57 μm |
Suportes de microscópios compatíveis | N-STORM | CSU-W1 SoRa |
ECLIPSE Ti2-E Inverted | yes | yes |
ECLIPSE Ti2-A Inverted | no | yes |
ECLIPSE Ti2-U Inverted | no | yes |
*Esses valores são fornecidos como referência aproximada. O desempenho da resolução varia dependendo das condições exatas. As estimativas de resolução não são mostradas para dimensões nas quais uma melhora não é esperada.
Literatura relacionada
Discussão de Aquisição de Imagem em Nanoescala
Encontrando o método de super-resolução apropriado para você
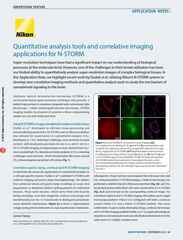
Análise quantitativa de espinho dendrítico utilizando série Z em 3D-SIM, 35 etapas, faixa Z: 4,2 um
Tempo de exposição: 100 ms, intervalos de 120 segundos
Lapso de tempo: 11 vezes
Comprimento de onda de excitação: 488 nm
Informações da amostra: Espinha dendrítica em neurônio do hipocampo de camundongo expressando GFP
Cortesia de: Dr. Yutaro Kashiwagi e Dr. Shigeo Okabe, Department of Cellular Neurobiology, Graduate School of Medicine and Faculty of Medicine, The University of Tokyo.
As técnicas de imagem de super-resolução fornecem uma melhoria da resolução para além do limite de difração. Entretanto, cada uma também tem suas próprias limitações e compensações, que devem ser bem compreendidas na busca pela técnica mais adequada para sua pesquisa.
Em primeiro lugar, as taxas de aquisição de super-resolução são geralmente mais lentas do que as técnicas tradicionais. A aquisição de imagem com N-STORM é difícil para aplicações que envolvam células vivas devido à taxa de aquisição mais lenta (quase universalmente exigindo mais de um segundo por frame). STORM e outras técnicas SMLM fornecem uma melhora na resolução, mas são compatíveis com um número limitado de fluoróforos, muitos dos quais requerem sistemas-tampão especializados incompatíveis com células vivas.
O Yokogawa CSU-W1-SoRa é mais adequado para imagens de células vivas em super-resolução, pois suporta taxas de aquisição de imagens mais rápidas (superiores a 15 FPS) e pode ser usado com fluoróforos convencionais sem sistemas de tampão específicos.
Lentes objetivas de alto desempenho para super-resolução
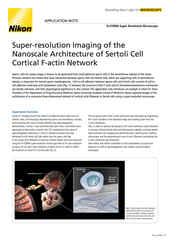
Lente objetiva da Nikon com colar de correção automatizada, montada em um microscópio invertido Ti2-E.
Um dos fatores mais críticos no que diz respeito à maximização da resolução óptica é a escolha da lente objetiva. Isso se aplica tanto à super-resolução quanto a outras técnicas de aquisição de imagem.
A abertura numérica (NA) da lente objetiva deve ser a mais alta possível para o meio de imersão apropriado. As lentes objetivas para microscópio da série Super-Resolution da Nikon incluem a CFI SR HP Apochromat TIRF 100XC Oil (imersão em óleo, NA = 1,49), a CFI SR HP Plan Apochromat Lambda S 100XC Sil (imersão em silicone, NA = 1,35) e a CFI SR Plan Apocromata IR 60XC WI (imersão em água, NA = 1,27). Essas objetivas fornecem algumas das NAs de nível mais alto em suas respectivas classes.
As objetivas da série Super-Resolution selecionadas estão disponíveis com um colar de correção automática, que permite um ajuste muito fino de correção de aberração esférica sem necessidade de ajuste manual, garantindo uma resolução de nível mais alto e possibilitando a aquisição de imagem 3D.
Resolução aprimorada – ultrapassando os limites das tecnologias tradicionais
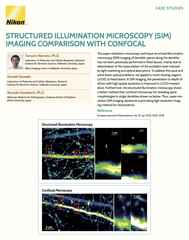
Imagens confocais de varredura pontual de cílios cocleares. Exibições XY e XZ com (direita) e sem (esquerda) configurações de resolução aprimoradas aplicadas.
Às vezes, a resolução necessária para responder à sua pergunta não está muito além da convencional e, portanto, pode não exigir algumas das compensações essenciais aos métodos de super-resolução. Nesse caso, recomendamos que você considere o potencial do que chamamos de aquisição de imagem confocal de “resolução aprimorada”.
O que é a aquisição de imagem confocal de resolução aprimorada? O ponto chave é entender que o microscópio confocal tradicional já é capaz de um certo grau de melhoria de resolução para além do que é possível utilizando um microscópio de campo amplo típico, com um limite teórico de ~140 nm (XY) sendo bem descrito. No entanto, atingir esse limite requer o uso de uma abertura de pinhole infinitamente pequena. Felizmente, na prática, um tamanho de pinhole de ~0,5 AU pode ser combinado com a deconvolução iterativa 3D pós-aquisição para se aproximar desse limite, com uma resolução de ~160 nm (XY) sendo um objetivo realista para uma variedade de condições de aquisição de imagem.
Os microscópios confocais de varredura pontual AX / AX R da Nikon são capazes de aquisição de imagem de resolução aprimorada. As vantagens incluem a capacidade de detectar com precisão a maioria dos fluoróforos de espectro visível e de permitir a aquisição simultânea de até quatro canais espectrais. O pinhole é continuamente variável e tem um formato hexagonal (em vez de quadrado), o que possibilita um ajuste mais preciso. Com o modelo confocal de varredura ressonante AX R, é possível adquirir imagens a uma taxa de vídeo de 30 FPS ou mais rápido, se beneficiando, ainda, da resolução aprimorada.
Glossário
- Canais espectrais suportados
- Referente ao número de possíveis canais espectrais (coloridos) que são suportados (assumindo uma linha de laser para cada tipo de fluoróforo).
- Limite relativo de profundidade da aquisição de imagem
- Isso indica a faixa de profundidade Z aproximada (axial) dentro da qual o sistema indicado pode fornecer imagens com bom seccionamento óptico e boa relação sinal-ruído. Esse valor pode ser bastante variável e depende muito das propriedades ópticas da amostra e do recipiente, bem como da marcação.
- Limite relativo de resolução óptica
- Limite prático de resolução do sistema fornecido. O valor da resolução lateral (XY) é normalmente diferente do valor da resolução axial (Z). Se um valor de resolução Z não é mostrado, nenhuma melhora é fornecida nesse plano.
- Suportes de microscópios compatíveis
- Referente aos modelos de suportes de microscópios da Nikon que são compatíveis com cada sistema.
- Taxa de aquisição de imagem suportada
- As taxas são mostradas como frames por segundo (FPS).
- Área máxima de aquisição de imagem
- O maior campo de visão (medido no espaço amostral) suportado pela técnica, utilizando o fator de ampliação especificado da lente objetiva.
- Início
- Aplicações
- Ciências da vida
- Aquisição de Imagem em Nanoescala