- es Change Region
- Global Site
- Casa
- Aplicaciones
- Ciencias Biológicas
- Imágenes a nanoescala
Imágenes a nanoescala
Durante cientos de años, la resolución de la microscopía óptica estuvo limitada fundamentalmente por la difracción, considerándose ~200 nanómetros (nm) como el límite aproximado en XY. Esto puede ser suficiente para observar células individuales y muchas características sub-celulares, pero es insuficiente para resolver detalles minúsculos en la escala de sub-orgánulos y biomoléculas individuales, que a menudo tienen dimensiones en un solo nm.
La historia reciente ha sido testigo de la invención de numerosos métodos de imagen óptica de “súper-resolución”, explotando diferentes estrategias para eludir el límite impuesto por la difracción. La importancia de la superresolución fue reconocida con el Premio Nobel de Química de 2014 y ya ha contribuido a varios descubrimientos, como la estructura del andamio periódico axonal.
Productos para la obtención de imágenes a escala nanométrica
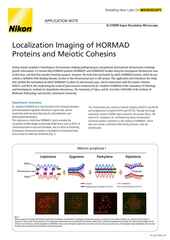
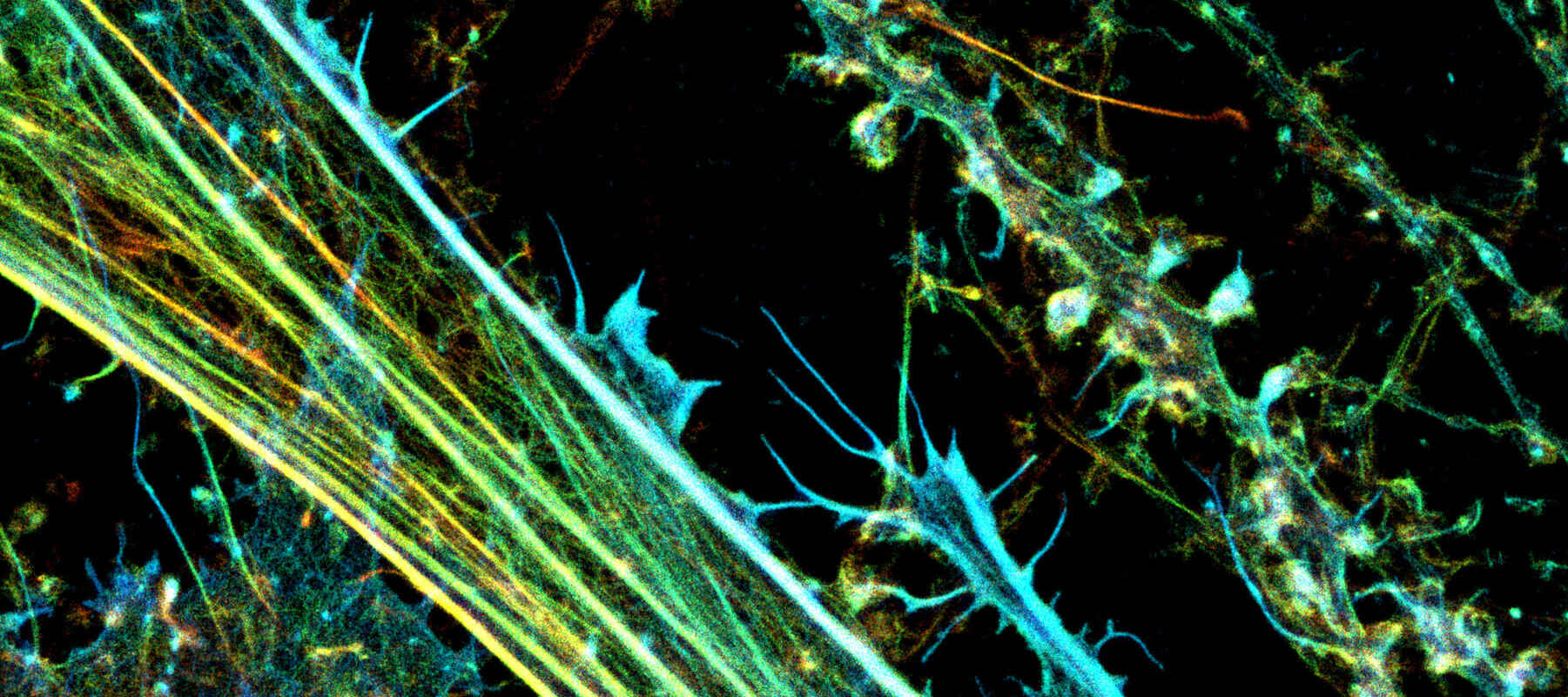
Imagen 3D-STORM de un cultivo neuronal con actina marcada con fluorescencia (codificada por colores para la profundidad), adquirida con un sistema Nikon N-STORM por el Prof. Christophe Leterrier (CR1 CNRS).
El sistema de microscopio de superresolución N-STORM de Nikon proporciona la resolución más alta de los sistemas ofrecidos por Nikon, aproximadamente un orden de magnitud mayor en comparación con la epifluorescencia de campo amplio en XYZ. El N-STORM está configurado en el microscopio invertido Ti2-E, que proporciona alta estabilidad gracias al sistema de mantenimiento de enfoque Perfect Focus System 4 (PFS4), que también se utiliza para movimiento axial fino para nuestro modo de imagen STORM con apilamiento en Z. lo que permite obtener imágenes de volúmenes de hasta ~5 µm de espesor. Las imágenes convencionales de fluorescencia de reflexión interna total (TIRF) también son posibles con el N-STORM.
El sistema de microscopio de superresolución N-SIM S utiliza un modulador de luz espacial para cambiar rápidamente los patrones de interferencia, proporcionando un aumento de velocidad tanto para los modos de 9 imágenes (2D-SIM, TIRF-SIM) como para los de 15 imágenes (3D-SIM). La SIM de 9 imágenes se puede realizar a velocidades de hasta 15 fotogramas por segundo (FPS), compatible con muchas aplicaciones de obtención de imágenes de células vivas. TIRF-SIM proporciona un aumento de resolución adicional en (XY), junto con el corte óptico de la microscopía TIRF. El sistema de microscopio de superresolución N-SIM E es un modelo SIM más rentable para imágenes 3D-SIM y proporciona la misma mejora de resolución que el N-SIM S.
El sistema confocal de barrido de campo de súper resolución SoRa CSU-W1 de Yokogawa es un instrumento confocal de barrido de campo que integra un disco de microlente de emisión para lograr una súper resolución mediante la reasignación óptica de píxeles. Dado que el CSU-W1 SoRa utiliza un diseño de barrido de campo, la adquisición de imágenes es rápida.
●: Incluido, ⚬: Opcional
| N-STORM Sistema de microscopio de súper resolución |
N-SIM S Sistema de microscopio de súper resolución |
N-SIM E Sistema de microscopio de súper resolución |
Yokogawa CSU-W1 SoRa Confocal de Barrido de campo |
|
|---|---|---|---|---|
| Límite de resolución óptica relativa | ~20 nm (XY)* ~50 nm (Z)* |
~115 nm (XY)* ~86 nm (XY; modo TIRF-SIM)* ~269 nm (Z; modo SIM 3D)* |
~115 nm (XY)* ~269 nm (Z; modo SIM 3D)* |
~120 nm (XY)* |
| Límite de profundidad de imagen relativa | ~ 5 μm | ~ 10 – 20 μm | ~ 10 – 20 μm | ~ 50 – 100 μm |
| Tasa de adquisición de imágenes compatible | ~0.1 FPS (adquisición de hasta 500 Hz de fotogramas de una sola imagen) |
~15 FPS (Solo 2D-SIM y TIRF-SIM) |
~1 FPS (todos los modos) |
~30+ FPS (limitado solo por la relación señal-ruido, la velocidad de rotación del disco y la tasa de lectura de la cámara) |
| Canales espectrales compatibles | 3 | 6 | 3 | 6 |
| Área máxima de adquisición de imágenes | 80 x 80 μm (utilizando un objetivo 100X) |
66 x 66 μm (utilizando un objetivo 100X) |
66 x 66 μm (utilizando un objetivo 100X) |
61 x 57 μm (utilizando un objetivo de 100X con una lente de aumento de 2,8X) |
| Bases de microscopio compatibles | N-STORM | N-SIM S | N-SIM E | CSU-W1 SoRa |
| ECLIPSE Ti2-E Microscopio invertido | yes | yes | yes | yes |
| ECLIPSE Ti2-A Microscopio invertido | no | no | no | yes |
| ECLIPSE Ti2-U Microscopio invertido | no | no | no | yes |
*Estos valores se proporcionan como una referencia aproximada. El rendimiento de la resolución variará dependiendo de las condiciones exactas. No se proporcionan estimaciones de resolución para las dimensiones en las que no se espera una mejora.
Literatura relacionada
Discusión sobre la adquisición de imágenes a nanoescala
Cómo encontrar el método de superresolución adecuado para usted
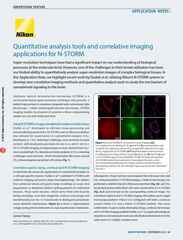
Análisis cuantitativo de la columna vertebral con Z-stack de 3D-SIM, 35 pasos, rango Z: 4,2 um
Tiempo de exposición 100 ms, intervalos de 120 s
Time-lapse de 11 veces
Longitud de onda de excitación 488 nm
Información de muestra: Espina dendrítica en neurona del hipocampo de ratón que expresa GFP
Película cortesía de: Dres. Yutaro Kashiwagi y Shigeo Okabe, Departamento de Neurobiología Celular, Facultad de Medicina y Facultad de Medicina de la Universidad de Tokio.
Las técnicas de obtención de imágenes de superresolución proporcionan una mejora de la resolución más allá del límite de difracción, pero cada técnica también tiene sus propias limitaciones y concesiones que deben entenderse bien para determinar cuál es la más adecuada para su investigación.
En primer lugar, las tasas de adquisición de súper resolución son generalmente más lentas que las técnicas tradicionales. La generación de imágenes con N-STORM es difícil de aplicar en células vivas debido a la tasa de adquisición más lenta (que requiere casi universalmente más de un segundo por cuadro). STORM y otras técnicas SMLM brindan la mayor mejora en la resolución, pero son compatibles con un número limitado de fluoróforos, muchos de los cuales requieren sistemas de búfer especializados que no son compatibles con las células vivas.
La N-SIM S y la Yokogawa CSU-W1-SoRa son más adecuadas para la adquisición de imágenes de células vivas de súper resolución, ya que admiten tasas de imágenes más rápidas (15 FPS para N-SIM S, más altas para CSU-W1-SoRa) y se pueden usar con fluoróforos convencionales sin sistemas tampón específicos.
Lentes de objetivo de alto rendimiento para superresolución
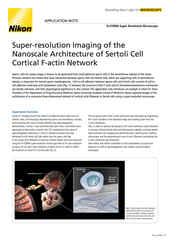
Lente de objetivo de collar de corrección automatizado de Nikon montada en un microscopio invertido Ti2-E.
Uno de los factores más críticos con respecto a maximizar la resolución óptica es la elección de la lente del objetivo. Esto se aplica tanto a la superresolución como a otras técnicas de obtención de imágenes.
La apertura numérica (NA) de la lente del objetivo debe ser lo más alta posible mientras se siga utilizando un medio de inmersión adecuado. Las lentes de objetivo de microscopio de la serie Super-Resolution de Nikon incluyen CFI SR HP Apochromat TIRF 100XC Oil (inmersión en aceite, NA = 1,49), CFI SR HP Plan Apochromat Lambda S 100XC Sil (inmersión en silicona, NA = 1,35) y CFI SR Plan Apocromático IR 60XC WI (inmersión en agua, NA = 1,27). Estos objetivos proporcionan algunas de las NA de más alto nivel en sus respectivas clases.
Los objetivos seleccionados de la serie Super-Resolution están disponibles con un collar de corrección automático, lo que permite un ajuste muy fino de la corrección de la aberración esférica sin ajuste manual, lo que garantiza la resolución de nivel más alto y el rendimiento de la adquisición de imágenes 3D posibles.
Resolución mejorada: superando los límites de las tecnologías tradicionales
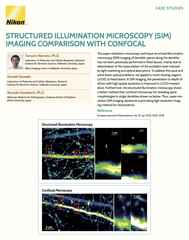
Imágenes confocales de barrido por puntos de cilios cocleares. Vistas XY y XZ con (derecha) y sin (izquierda) configuración de resolución mejorada aplicada.
A veces, la resolución necesaria para responder a su pregunta no va mucho más allá de lo convencional y, por lo tanto, es posible que no necesite algunas de las concesiones exigidas por los métodos de superresolución. En tal caso, le recomendamos que considere el potencial de lo que llamamos imágenes confocales de “resolución mejorada”.
¿Qué son las imágenes confocales de resolución mejorada? El punto clave a entender es que el microscopio confocal tradicional ya es capaz de mejorar un cierto grado de resolución más allá de lo que es posible con un microscopio de campo amplio típico, con un límite teórico de ~140 nm (XY) bien descrito. Sin embargo, alcanzar este límite requiere el uso de una abertura de diafragma infinitamente pequeño. Afortunadamente, en la práctica, un tamaño del diafragma de ~0,5 Airy Units se puede combinar con la deconvolución iterativa 3D posterior a la adquisición para acercarse a este límite, con una resolución de ~160 nm (XY) que es un objetivo realista para una variedad de condiciones de captura de imagen.
Los microscopios confocales de barrido por puntos AX / AX R son capaces de obtener imágenes de resolución mejorada. Las ventajas incluyen poder ajustar con precisión la detección de la mayoría de los fluoróforos del espectro visible y permitir la adquisición simultánea de hasta cuatro canales espectrales. El diafragma es continuamente variable y tiene forma hexagonal (en lugar de cuadrada), lo que permite un ajuste más preciso. Con el modelo confocal de escaneo resonante AX R, es posible obtener imágenes a velocidad de video (30 FPS) y más rápido mientras se beneficia de una resolución mejorada.
Glosario
- Bases de microscopio compatibles
- Se refiere a los modelos de base de microscopio Nikon que son compatibles con cada sistema.
- Canales espectrales compatibles
- Esto se refiere a la cantidad de posibles canales espectrales (color) que se proporcionan (suponiendo una línea láser para cada tipo de fluoróforo).
- Límite de profundidad de imagen relativa
- Esto indica el rango de profundidad Z (axial) aproximado dentro del cual el sistema indicado puede producir imágenes con suficiente calidad de seccionamiento óptico y relación señal/ruido. Este valor puede ser bastante variable y depende en gran medida de las propiedades ópticas de la muestra y el recipiente, así como de la tinción.
- Límite de resolución óptica relativa
- El límite de resolución práctico del sistema dado. El valor de la resolución lateral (XY) suele ser diferente al de la resolución axial (Z). Si no se proporciona un valor de resolución Z, entonces no se proporciona ninguna mejora en esa dimensión.
- Tasa de adquisición de imágenes compatible
- Las tasas se muestran como fotogramas por segundo (FPS).
- Área máxima de adquisición de imágenes
- El campo de visión más grande (medido en el espacio de muestra) compatible con la técnica utilizando el factor de aumento de la lente del objetivo especificado.
- Casa
- Aplicaciones
- Ciencias Biológicas
- Imágenes a nanoescala